全球首个“完美婴儿”3岁了,基因筛选引热议:真正的科技与狠活!
1997年的科幻电影《GATTACA》描绘了这样一个被严格按照基因划分等级的世界——精英的孩子会在基因工程加工,筛选后出生,经过筛选的完美孩子,将会从事高精尖的工作夫妇们可以通过基因技术,生出拥有完美基因的孩子。而付不起优生费的父母只能通过自然受孕分娩生孩子,接受疾病,性格甚至寿命长短的随机性,这些孩子长大后也只能从事一些低端工作。故事主角文森特是一个自然受孕而被生下的孩子,他从一出生就被检测出了这样的结果:神经性疾病可能性60%
狂躁症可能性42%
注意力无法集中可能性89%
心脏病概率99%
有过早死亡可能性,预期寿命:30.2年面对这样一个“残次品”,文森特的父母通过筛选基因来拥有第二个孩子。正如医生所说,这个孩子的基因仍是来自父母,不过是最佳基因。就这样,拥有父母完美基因的弟弟安东来到了世界上。果然,兄弟俩的成长史证明了,基因好的孩子就是牛!安东高、漂亮、聪明,是父母的手中宝;文森特集矮丑矬于一身,爸妈也不怎么待见他。现实生活中有多少人幻想过通过技术手段,获得一个按照自己意愿设计的,更健康、更聪明、更好看的孩子?事实上,这可能不只是狂想,因为已经有人付诸了行动。这个人叫做拉法尔,来自美国北卡罗来纳州 Novant Health Forsyth 医疗中心,是一名神经科医生,他创造了世界上第一个通过「多基因评分」筛选诞生的孩子。被称为“完美婴儿”的奥蕾拉也即将健康成长至3周岁。拉法尔和现任妻子都已年过五十,两人此前分别离婚后,带着各自的孩子重组了现在的家庭。尽管已经属于高龄受孕,但他们还是决定通过辅助生殖技术,再生一个属于两个人的孩子。考虑到高龄生育可能会给孩子带来更高的遗传病风险,拉法尔看了许多研究资料,一篇发布于《麻省理工科技评论》的文章吸引了他的注意。这篇文章提到,基于多基因评分的胚胎选择ESPS技术可以筛查疾病、选择胚胎。ESPS 是多基因评分(polygenic risk scores, PRSs)的一个应用方向,是在辅助生殖过程中通过评分的方式,对胚胎进行多基因相关性状的筛选,从而选择最可能符合需求(比如患某种疾病风险最低、高智力水平概率最高等)的胚胎,移植入母体进行生育。目前这一技术除了用于科学研究,主要潜力还是在于实现多基因遗传病的一级预防 。
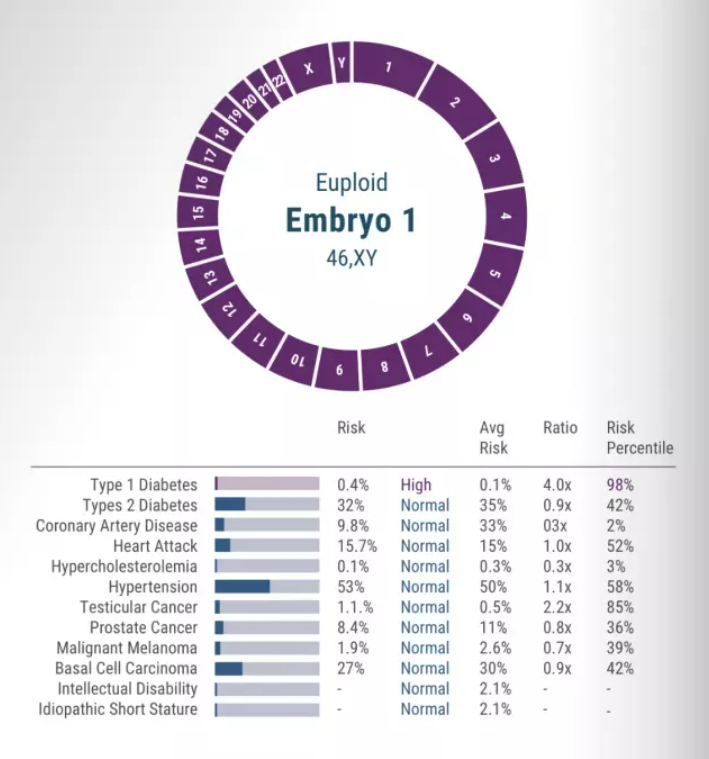
拉法尔虽然临床从事的是神经科工作,但早年也曾取得遗传学博士学位。他从ESPC中,看到了给孩子选择完美基因的机会。尽管该技术是否有效、是否安全、是否应该用于优生都没有定论,拉法尔仍坚持自己的想法。他找到了一家体外受精技术供应商,和另一家愿意提供胚胎检测服务的公司,与试管婴儿医生一起研究,从自己的体外受精胚胎细胞中,提取DNA样本、进行测序分析、构建基因图谱、解读遗传信息,从而预测孩子出生后可能的健康和智力水平。最终,他们从16个胚胎中选出5个进行基因检测。这5个胚胎中,有一个因检测出染色体异常直接舍弃,余下4个则获得了整体的胚胎评分。在拉法尔的努力下,他的小女儿奥蕾拉成为了世界上第一个经ESPC诞生的完美婴儿。而在2022年8月,中国首例PGT-P试管婴儿诞生,迈出多基因遗传病源头防控第一步。受试者家族中有高发的II型糖尿病史,而II型糖尿病正是多基因遗传病,他们想要一个没有II型糖尿病风险的宝宝,PGT-P带来了希望,经过数个月的努力,经过患者知情同意,他们选择移植了较低糖尿病风险的1号胚胎。最终迎来了一名健康的男婴。目前无论是具备普通的PGT还是PGT-P技术资质的诊所都只能用其来避免严重的疾病和辅助不育治疗,其他的性状筛选及性别选择等是被严格禁止的。
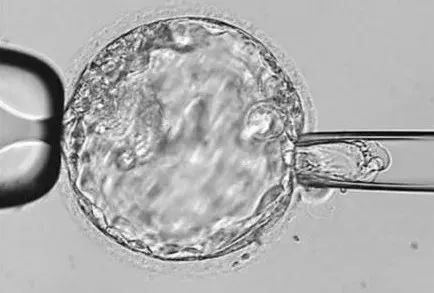
总的来说,PGT-P等基因检测技术确实可能有助于减少因疾病给一个家庭造成不幸的可能,但是另一方面,伦理和道德规范的模棱两可也为这一技术的应用带来隐患。虽然目前针对人类的多基因评分虽然还处于研究阶段,但已有在临床或商业中,为某些疾病的基因风险提供检测的服务。而反观胚胎选择,其实也不是新鲜事。对于受孕困难,或患有高致死、致畸、致残风险的严重遗传疾病(如染色体病、单基因病)的父母,采集精子和卵子在体外一次长成几个胚胎,选择生长情况最佳的植入子宫,试管婴儿技术早就是成熟应用的方案。胚胎植入前遗传学检测PGT,又称为第三代试管婴儿, 是指在胚胎移植前,对体外受精的胚胎进行遗传物质分析,排除携带已知致病基因的胚胎,将从基因层面优选后的胚胎移植入宫腔,不仅能够提高体外受精-胚胎移植技术的成功率,而且避免了流产,治疗性引产带给女性身体及精神上的创伤。世界范围内,最早依靠此技术诞生的婴儿可以追溯到1990年。英国学者首次利用鉴定Y染色体来减少生育母源性X连锁隐性疾病患儿的机会。我国的第一例于1999年诞生。PGT-A胚胎植入前非整倍体遗传学筛查;
PGT-M胚胎植入前单基因遗传学检测;
PGT-SR胚胎植入前染色体结构变异遗传学检测。
每一类都有其针对性的适应症。抛开繁复的专业术语,简单来讲,该技术主要是在胚胎移植的基础上,针对胚胎染色体异常进行诊断和筛查。染色体异常是造成早期流产和IVF反复失败的重要原因。染色体畸变既可能自然发生,也可由物理、化学和生物因素诱变而产生。常见的诱发因素包括辐射、病毒(如风疹、巨细胞、艾滋病毒等)感染及化学物质(如某些杀虫剂、铅汞苯等)。当然可能由亲代遗传而来,孕妇高龄也是导致新生儿染色体畸形的原因之一。
染色体异常包含结构和数目畸变两大类,其中数目畸变又包含了整倍体,非整倍体和嵌合体三类,而PGT-A则是针对临床上最常见的染色体畸变类型-非整倍体进行诊断,其中最著名的21三体综合征,又称唐氏综合征,即21号染色体多出一条。有研究显示,通过对早期自然流产胚胎的遗传学分析,发现染色体异常的概率可达50-60%。女方高龄(年龄≥38岁);
反复IVF种植失败(移植3次及以上,或移植高评分卵裂期胚胎数4-6个,或高评分囊胚数3个及以上均失败);
反复妊娠失败(不明原因自然流产2次及以上);
严重畸精子症的患者。
有研究表明,对反复着床失败患者进行PGT-A检测后,其临床妊娠率可达到非RIF患者相近的水平(分别为68.3%和70.5%),而未进行PGT-A的RIF患者的临床妊娠率仅为21.2%。因此,PGT-A旨在提高活产率、降低不良妊娠率,预防染色体综合征,出生缺陷的发生。染色体的结构畸变更为复杂精细,可分为缺失、重复、倒位、异位等等。若夫妻任何一方或双方携带有异常结构的染色体,生育过染色体异常疾病患儿的夫妇均可以进行PGT-SR的检测,其目的是降低子代发生染色体结构异常的风险。通常来讲,其适用于经核型分析诊断为异常的夫妻任何一方或双方。例如,染色体的相互易位及罗氏易位,又称为平衡易位,并没有遗传物质的丢失,智力、表型与正常人并无区别,然而孕育子代时,产生的配子由于不平衡,可能引起生育力下降、流产、胚胎发育异常等问题。通常采用原位杂交或高通量测序技术进行PGT-SR的检测。针对致病基因明确的单基因病,如地中海贫血、血友病、杜氏肌营养不良、多囊肾等。
此类遗传病多数为隐性遗传病,即两条同源染色体上均存在相同致病基因、或男性X染色体存在致病基因(X连锁)时才会发病的遗传病,仅一条染色体携带致病基因(X连锁除外)时不发病或症状不明显,称为致病基因携带者。
1、夫妻任一方或双方携带严重疾病的易感突变基因,如遗传性乳腺癌卵巢癌的BRAC1、BRAC2致病突变。好莱坞影星安吉丽娜朱莉,由于遗传了家族突变的BRCA1基因,导致其患乳腺癌和卵巢癌的风险远高于正常人。因此,她接受了预防性的乳房切除和卵巢切除。而PGT这一技术能够提前筛查出此种突变,其家族子代不仅患病风险大大降低,也无需进行预防性的手术切除,实现了在胚胎阶段就阻断突变基因的遗传。2、人类白细胞抗原(HLA)配型:曾生育过需要进行骨髓移植治疗的严重血液系统疾病患儿的夫妇,可通过PGT-M选择生育一个和先前患儿HLA配型一致的同胞,通过从新生儿脐带血中采集造血干细胞进行移植,救治患病同胞。自1978年首例试管婴儿诞生及随后40多年来该领域持续取得的突破性进展,促进了以体外受精为基础的ART技术在临床的广泛应用,提升了人类孕力,也造福了全球范围内千千万万个家庭。
繁衍后代,终究是生命的一种本能。即便在生育成为难题的当下,每个人的生育选择权利仍应得到尊重。
虽然辅助生殖技术不是解决生育问题的万能灵药,但它终究留下了希望。合理、规范地应用此类技术必将能继续造福社会、惠及更多人群。现在技术依然在不断进步,相信未来还能见证更多的奇迹时刻。